一、放射醫學影像3D成像應用與技術簡介
常用放射醫學3D影像形成方式包括核磁共振造影(Magnetic Resonance Imaging, MRI)、CT電腦斷層掃描 (Computed Tomography, CT)、正子電腦斷層掃描(Positron Emission Tomography, PET)、單光子電腦斷層掃描(single photon emission CT, SPECT)等,以非侵入式的方式得到人體組織結構的三維圖像,為現今醫學診斷癌症、心血管病變、內出血、神經病變等疾病的重要工具,提供設備的主要廠商有GE Healthcare, Siemens Healthineers, Philips, Canon等。為了以非侵入式的方式呈現人體內部構造與狀態,3D醫學影像利用外加物理能量在體內組織作用,再以數值分析所產生的訊號來重建體內構造的影像。各類造影應用的目的與優缺點綜整如表1。
表1 各類放射科3D影像應用的目的與優缺點
|
|
MRI
|
CT
|
核子醫學 (PET/SPECT)
|
|
主要用途
|
腦部、脊椎、血管、心臟、肝腎脾臟、乳房、關節、肌肉與韌帶組織等之病變檢查
|
胸腹與骨盆腔器官檢查、癌症篩檢、骨骼等部位創傷、心臟與各部位血管攝影
|
癌症、心血管灌流、神經性病變等早期檢測與治療追蹤
|
|
優點
|
無放射線、軟組織解析對比佳、可任意斷面掃描、可收集解剖構造與組織成分資訊、可做功能性造影
|
造影速度快、空間分辨力佳
|
分子層次功能性造影、病變檢出靈敏度與特異性高
|
|
限制
|
造影時間長且噪音大、骨骼及鈣化組織細節解析度較差、磁場限制不適用於有金屬植入物病人及不易與其他治療儀器整合、機台昂貴
|
放射劑量高、無法收集功能性資訊、軟組織對比不佳
|
造影時間長、需服用帶輻射之同位素追蹤劑、空間解析度低解剖資訊有限、檢測成本高
|
資料來源:工研院產科國際所 ITIS研究團隊整理 (2021/05)
MRI 造影利用體內組織水分的核磁共振(nuclear magnetic resonance, NMR)現象,透過儀器給與磁場,造影時利用磁場梯度來做空間編碼以區辨訊號來源,在訊號頻域k-space 的兩個維度分別做頻率編碼與像位編碼,量測給予磁場後含水組織氫原子共振所放射的電磁波,再經傅立葉轉換(Fourier Transform) 將訊號從頻域轉至空間域便可得到組織影像。MRI的優勢為成像不需要放射線,可針對診斷標的利用脈衝頻率與訊號量測時機等參數變化來強化不同組織之訊號差異,對軟組織有較好的解析能力。
其應用最大的限制為造影時間需時較長,同樣達到millimeter解析度的影像,CT造影只需要幾秒鐘,MRI造影卻要20分鐘或更長,減少MRI造影時間因此一直是機台廠商積極研發的方向。近年來各廠商推出以訊號壓縮理論為基礎的Compressed Sensing 以減少訊號擷取樣本數來加速,雖使造影時間可減少30-50%,但如同JPEG影像壓縮運算時需在壓縮比率與可還原資訊之間的取捨,在影像診斷靈敏度的權衡下,應用Compressed Sensing能壓縮的造影時間也因此有限。
CT電腦斷層掃描為目前最常用的3D醫學影像方法。其利用X-ray在特定軸面旋轉照射人體而由對向的偵測器接受訊號,藉內部組織對X射線的阻射率(attenuation)差異,不同照射角度透過人體後所測的訊號組合sinogram 便可用於重建斷層而造影。理論上當照射光路上的物質阻射率均勻訊號呈線性衰減、沒有散射及雜訊等完美條件下,將sinogram經由反投射計算(back projection)便可得到斷層影像。然而在臨床應用上完美條件並不易達成,但因計算簡單運算資源需求小,2009年以前臨床應用CT造影便以 FBP (filtered back projection),將sinogram 經high-pass filter再反投影為主要的成像方法。
隨著CT電腦斷層在臨床應用的日漸普及,CT造影所需高劑量X-ray可能造成病人危害的風險開始受到重視,低劑量X-ray 成像成為CT造影技術研發重點;此外,加上肥胖人口增多,以及CT造影設備進化的更加複雜,來自系統的干擾增多,低訊號雜訊比的狀況下FBP方法在成像品質的限制開始浮現。另一方面,電腦運算硬體方面的進步,低劑量X-ray造影以疊代影像重建影像(iterative reconstruction, IR)的相關技術於是快速發展,成為現今主要臨床應用CT機台成像的基本方法。這些IR方法將成像系統以及可能影響訊號產生的物理現象以多參數模型模擬,推算現擬成像結果所源自的sinogram訊號(圖1之2)再將其與實際量測訊號(圖1之1)比較,由兩者相較差異而更新成像模型(圖1之3-5),需多次迴圈來回修正來逐步減小量測與模擬之差距而得最終成像。
目前主要設備廠商所開發應用基於IR的演算法與前代FBP方法相較,在減少 23% 至 76% 的X-ray劑量下仍獲得相當品質的影像( Physica Medica 28:94-108)。然而可描述的成像系統的參數是有限的,IR方法雖可在低劑量造影下提供可做臨床診斷的影像品質,但與高劑量造影結果相比仍有突破空間。
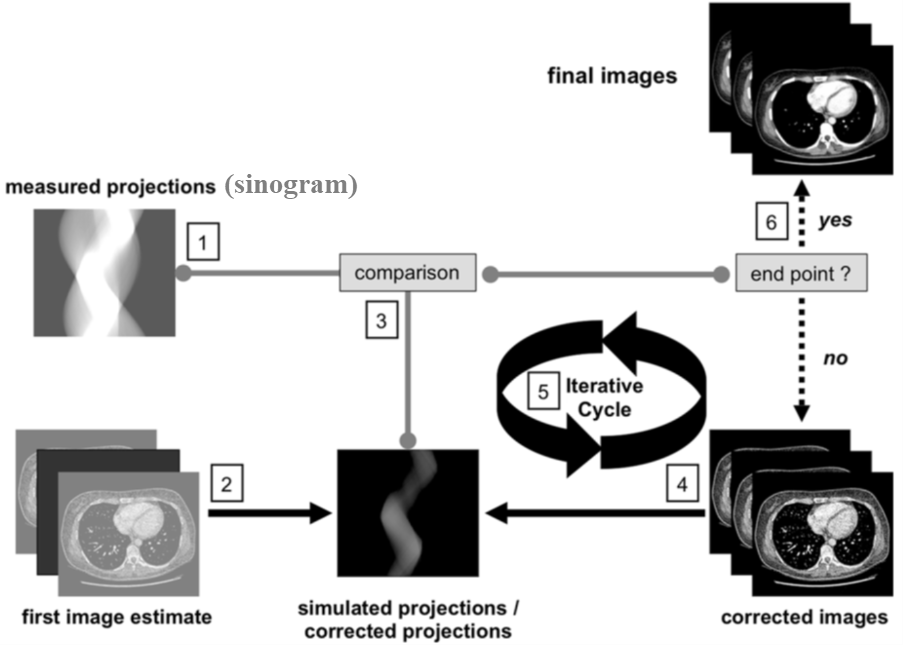
資料來源:Radiology (2015) 276:339-357
圖1 Iterative Reconstruction 方法電腦斷層影像重建之運算架構
核子醫學影像 PET 及SPECT成像原理與CT電腦斷層掃描類似,但訊號源為來自病患口服或注射的放射性同位素追蹤劑,進入體內後同位素衰變所產生的射線訊號透過人體而被體外的偵測器接收,其繞著人體從多個角度作直線掃描而產生sinogram,因此影像重建演算法發展亦類似CT以FBP或IR為基礎架構。PET與SPECT的差異在於SPECT使用的衰變的同位素,產生訊號經準直儀(collimator)過濾後由gamma camera紀錄;而PET使用β+衰變的同位素,所放出正子與周邊電子結合所產生的互毀反應(annihilation reaction) 會形成一對方向相反的射線,因此藉掃瞄並行事件(coincidence)可定位訊號源。由於同位素追蹤劑會聚集在特定標記位置或血流及代謝旺盛之處,核子醫學影像主要用用診斷病理或生理功能變化,解剖構造的資訊有限,因此現在核子醫學造影設備多與CT或MRI造影設備整合而產生資訊互補的影像。
二、人工智慧在放射科造影成像之產業應用現況
自人工智慧技術興起,放射科影像便成為熱門的應用領域,除了在影像分析診斷方面百家爭鳴,由深度學習自大量數據中探勘系統參數的方法也成為造影設備廠用來進化成像技術的重要工具,用於克服現有成像技術限制,開發能利用低放射劑量或加速造影的訊號來重建更高品質的3D影像。如GE Healthcare所開發的Deep Learning Image Reconstruction (DLIR, 品牌名TrueFidelity)及Canon 所開發的Advanced Intelligent Clear-IQ Engine (AiCE) 皆針對前節提到現今CT造影所使用的IR方法的限制而設計,於2019年先後獲美國FDA應用於其自家多個CT機型。兩家公司應用在MRI降雜訊處理的深度學習演算法亦皆於2020年經美國FDA核可搭配特定MRI機型,藉AI能由低SNR (signal-to-noise ratio) 訊號重建高解析度影像的能力而增取MRI影加速造影的空間。
(一) 深度學習革新低劑量CT造影成像品質
2019年4月GE Healthcare的DLIR成為第一個被美國FDA核准應用深度學習的造影重建演算法,除配備於GE 新推出的Revolution Apex CT 機台外,前代Revolution CT系列機台亦可升級使用,可應用於頭部、全身、心臟與血管的CT造影。GE前一代CT重建的IR方法 ASiR (Adaptive Statistical Iterative Reconstruction)利用訊號統計模型模擬,成像時以降雜訊為優化目標,然而由低劑量造影所重建的影像經降雜訊優化後紋理特徵(noise texture)常被放射科醫師認為不自然,且成像品質對照高劑量造影仍有改善空間。GE的AI的造影重建DLIR 開發過程以低劑量造影訊號為輸入資料,以同樣物件高劑量造影、FBP成像的影像為輸出標的而做深度學習(圖2),學習資料來自假體(phantom) 與實際臨床資料。所建構的Deep Neural Network (DNN) 成像模型應用在低劑量造影在不僅在降雜訊、提升Contrast-to-Noise Ratio、低對比物件偵測力等皆較FBP及ASiR佳,紋理特質亦較ASiR方法接近高劑量造影重建的結果。
臨床驗證的回溯性實驗中,利用含小區域病變之低對比影像的原始數據分別以兩種演算法重建做測試,60對造影結果經9位放射科醫師就影像清晰度、紋理特徵滿意度等項目評分,統計比較DLIR各方面皆優於前代的ASiR成像法。2020年底DLIR 進一步被獲准用於GE之雙能階CT能譜造影Gemstone Spectral Imaging,更利於將組織分解成以水、碘、鈣等不同物質為主的影像而分析,可增加病變偵測率與定位準確度,並減少金屬植入物造成的假影。
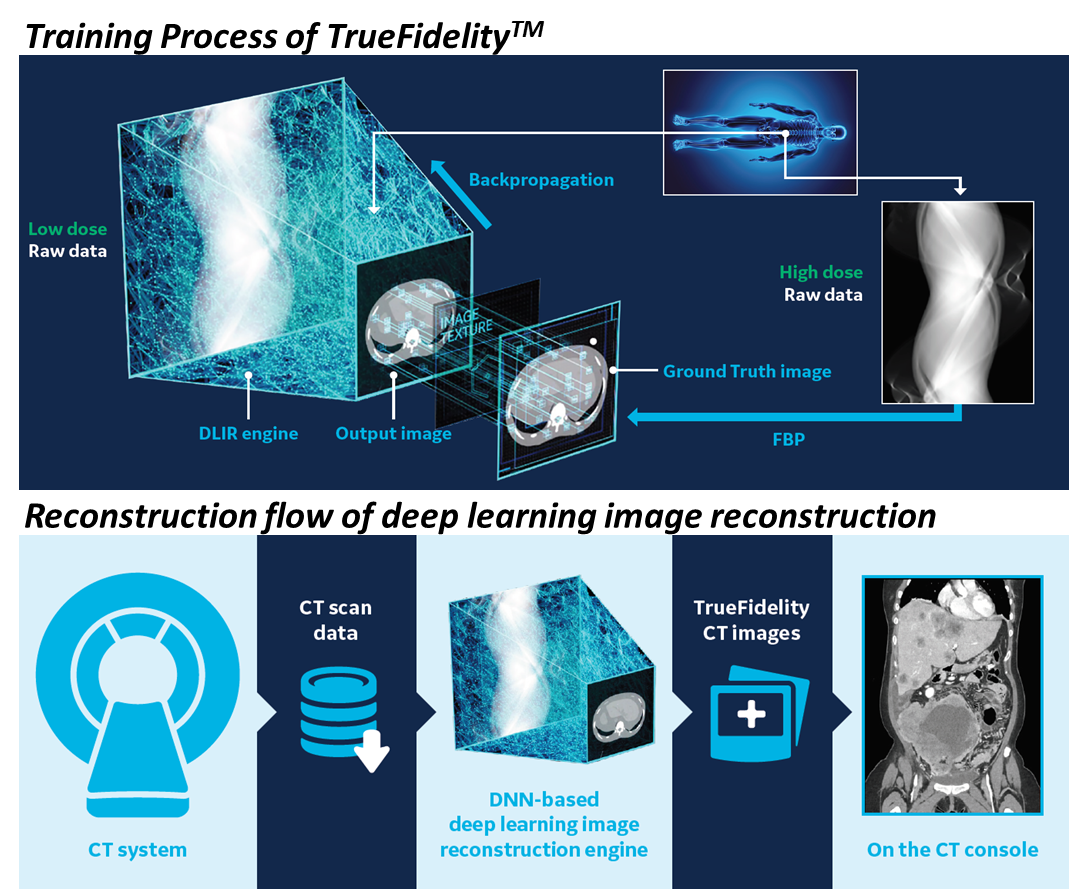
資料來源:GE Healthcare
圖2 GE Healthcare 之CT造影重建深度學習演算法的開發與應用
Canon 的深度學習CT影像重建演算法AiCE則先是在2019年10月在美核可搭配其超高解析度的新機型 Aquilion Precision用於腹腔與骨盆腔部位之造影。藉影像訊號特質客觀量測如Contrast-to-Noise Ratio、CT Number 正確率等評估,AiCE與其現用的IR方法AIDR 3D (Adaptive Iterative Dose Reduction 3D)相較下有較好的影像品質,提升對低對比物件偵測力,並有較佳的空間解析度。AiCE所採用與GE’s DLIR類似的建構策略,以低劑量造影訊號為輸入資料,但使用包含CT系統之機構物理、機構、統計、組織解剖等高複雜度參數模型為基礎之IR方法(Model-based Iterative Reconstruction, MBIR)所重建的影像為輸出標的,以Deep Convolutional Neural Network (DCNN)為架構做深度學習,學習資料亦來自假體與實際臨床資料。該MBIR方法雖能以較完善的模型描述成像條件因此能得到較佳的成像品質,但高度複雜運算所需的資源與時間限制了其在實際臨床的應用。
藉由深度學習,MBIR方法重建影像所需的參數因而可內含於所建構的DCNN模型,所訓練出的模型在應用上便可省去參數探索的計算而重建同等品質的影像。其進化版在2020年2月再獲准搭配其能階調變CT機型Aquilion ONE / PRISM,用於重建腹腔、骨盆腔、腹部、心臟、四肢、頭部及內耳的CT 能譜造影(Spectral Imaging)而做多物質影像分解分析,不同能階的影像在時間上與空間上的重疊更精確,使CT 能譜影像可於常規檢測進行。此外,Canon 在2020 年北美放射科醫學年會RSNA 亦展示AiCE 應用於其Cartesion Prime Digital PET/CT 機台,可在減少放射劑量、造影時間的狀況下同時提供高影像品質的結構與功能性造影而精準定位病變區,目前已送FDA進行上市審理。
(二) 藉深度學習提升快速MRI造影的品質
需在造影時間、訊號SNR比與影像解析度間擇一妥協,一直是MRI影像造影技術應用的議題;近年利用大量資料訓練、建立能由少數數據重建原始訊號之深度學習技術則在MRI造影技術發展上開啟了一個新的發展方向,利用AI使成像品質與MRI造影時間的同時改善的方案亦成為眾MRI設備廠積極研發的領域。其中前述Canon 的AiCE 產品在MRI的應用亦於2020年3月與7月分別在美獲准應用於Vantage Galan 3T 及Vantage Orian 1.5T MR設備,GE Healthcare 為MR造影優化所開發的 AIR Recon DL 則在2020年5月與9月分別獲美國FDA准用搭配於其3T 及1.5 T MR系統SIGNA Premier。
Canon 的AiCE在MR造影成像的應用方面以降雜訊為主要目標,同樣利用DCNN架構,利用高解析度影像加上雜訊來訓練模型區分訊號與雜訊以還原影像,用於訓練的影像為各種對比權重(T1, T2, FLAIR, PD)的腦部及膝部影像;實際造影應用時所訓練的DCNN 則將僅處理原始造影訊號高頻部分以保留影像對比資訊。經AiCE處理,即使造影時間縮減一半減少訊號擷取次數使仍可重建高品質;而同樣造影條件在盲測實驗下醫師普遍認為經AiCE處理的影像品質較佳。
此外,Canon在其AiCE Challenge網站提供由1.5T MR造影AiCE 成像的影像及3T MR造影但以原本成像方法之影像比較 (註: T, Tesla為磁感應強度單位,值越大造影訊號SNR比越好,但機台造價越高),半數以上的放射科醫師無法區分其中差異,意味未來醫院在MRI上設備的投資上有大幅節省的空間。
GE Healthcare 之MR造影優化的AI模型 AIR Recon DL 則經由與全球各地多個臨床中心合作開發與驗證,利用CNN(Convolutional Neural Network)深度學習架構,將影像原始訊號(k-space)經處理產生低解析度影像來訓練模型將訊號還原成高解析度影像,同時針對降雜訊及減少傅立葉轉換所產生的波紋偽影(註:轉換至空間域時因頻域訊號截斷所產生的誤差造成近邊界區的Gibbs ringing) 兩大目標優化。利用AIR Recon DL重建的影像有較銳利的邊緣,使用邊長為1.4-1.6倍的造影單位 in-plan voxel重建時影像亦可維持原本的解析度(註: 造影單位越大訊號積分累計越強,但空間解析度降低),因此在造影時間需求上或設備上都有了簡化的空間(圖3)。
臨床驗證實驗盲測21位來自不同國家11家醫院的放射科醫師檢視影像,一致認為在相同造影狀況下AIR Recon DL重建的影像有較清晰的邊緣與影像細節,診斷品質較佳。
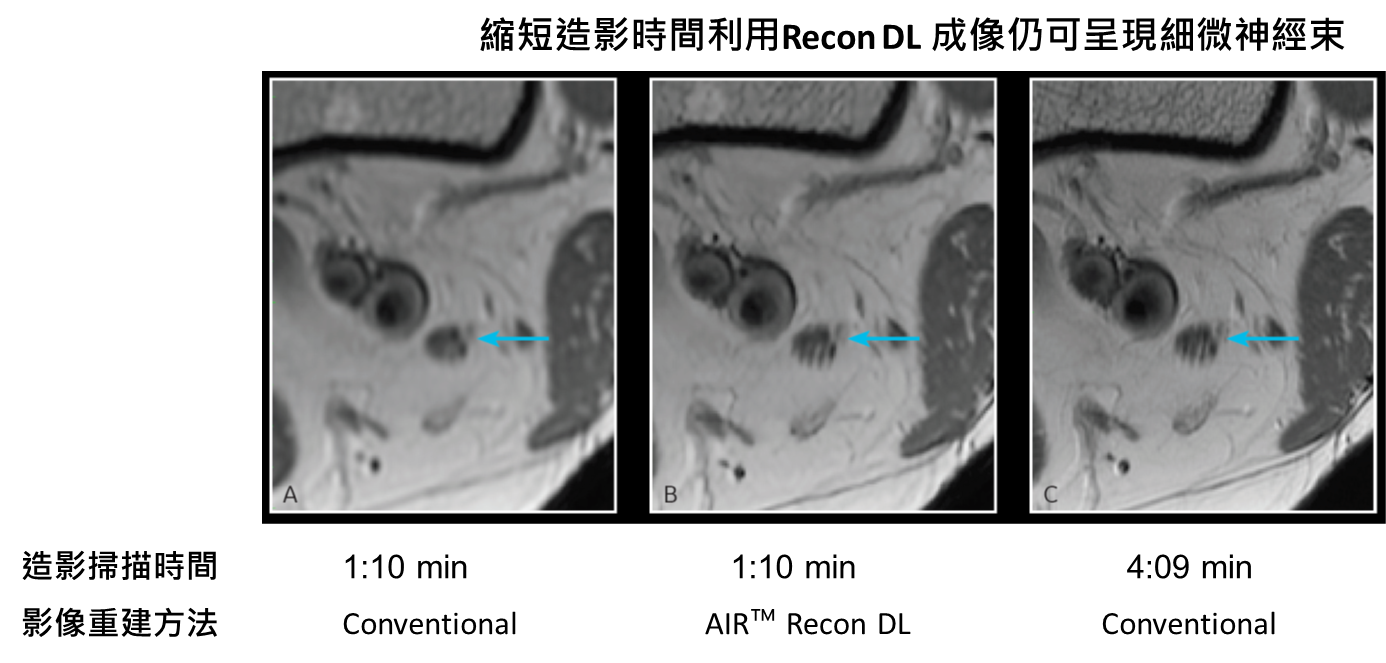
資料來源:GE Healthcare
圖3 GE Healthcare 之MRI造影重建AI演算法減少掃描時間仍可清晰成像
除Canon 與GE Healthcare 的MRI影像重建AI已獲上市外, Siemens Healthineers 在2020 年RSNA亦展示將搭配其1.5T與3T MR 機台的深度學習影像重建軟體Deep Resolve,功能訴求類似GE的AIR Recon DL,去雜訊與與減偽影雙管齊下,目前經由其數位平台供訂閱者試用中,預期可上市時間將不遠。另一MRI設備大廠 Philips 則與Intel合作開發結合深度神經網路與Compressed Sensing 快速成像的影像重建方法,由演算法及運算單元同時加速並維持影像品質,預期其下一代產品在成像速度與品質上將有別於現有上市機台的競爭力。
三、結論
觀測上述應用在放射醫學影像3D造影成像之AI產品策略,GE Healthcare 及Canon 除了搭配最新造影機型推出使用外,也皆布局讓前一代的機型可升級使用,既有的客戶不需重新採購設備也能藉軟體使機台升級。目前核可上市的影像重建AI皆不被允許再做模型參數修正,然而在產品上市使用後,廠商將可藉實際運行時收集的數據不斷提升模型的成像品質,未來軟體部分的產品週期將遠快於造影設備。GE Healthcare 因應此趨勢已先對CT 設備推出Smart Subscription 行銷方案,訂閱客戶將可即時享用最新的軟硬體功能,廠商則可藉經常性收入穩定營收,由軟體加值獲利的空間增大,預期將會對行之有年造影系統銷售模式帶動不小的變革。
近年來人工智慧在放射科影像應用發展百家爭鳴,放射科醫師普遍認為能增進病人安全、減少放射劑量或顯影劑、及提升影像品質的AI為最具臨床價值的技術應用;如新創公司Subtle Medical自2018起且便推出多項不限機台品牌強化MRI、PET成像後影像品質的AI軟體而受到相當矚目,但在缺乏原始機台訊號下造影還原程度相對受限,與機台獨立運行使用上也較為不便。
相較下GE Healthcare、Canon等跨國設備大廠所開發的3D影像重建AI皆直接由量測訊號著手,藉訓練模型辨識系統雜訊而做影像強化,在提升影像品質之外將更能進一步提升影像診斷靈敏度。內建於造影機台將使AI在臨床的應用會更快速普及,深度學習神經網路的技術優勢、限制與演算法的可靠度也將更能被普遍檢驗。特別是隨著機台使用次數增多,造影系統機構狀態的變化是否影響既有模型的造影品質,設備廠商又將如何管理上市後機台搭載的AI軟體產品將值得關注。
參考資料
1. The Evolution of Image Reconstruction for CT—from Filtered Back Projection to Artificial Intelligence. European Radiology (2019) 29:2185–2195
2. Deep Learning for Tomographic Image Reconstruction. Nature Machine Intelligence (2020) 2:737–748
(本文作者為工研院產科國際所執行產業技術基磐研究與知識服務計畫產業分析師)