:::
產業技術評析

當標靶蛋白降解劑碰上抗體 - 淺析萌芽中的 DACs(Degrader Antibody Conjugates)發展現況
發表日期:2023-12-20
作者:游佩芬(工研院)
摘要:
抗體藥物複合體(Antibody Drug Conjugates, ADCs)技術領導藥廠Seagen在2023年9月宣布以高達6,000萬美金的頭期款(upfront payment)與標靶蛋白降解劑 (Target Protein Degraders, TPDs)藥物開發公司Nurix Therapeutics(以下簡稱Nurix)簽下多年合作開發協議。
全文:
一、知名ADCs藥廠Seagen以高達6,000萬美金的頭期款與Nurix Therapeutics合作開發新型藥物DACs
抗體藥物複合體(Antibody Drug Conjugates, ADCs)技術領導藥廠Seagen在2023年9月宣布以高達6,000萬美金的頭期款(upfront payment)與標靶蛋白降解劑 (Target Protein Degraders, TPDs)藥物開發公司Nurix Therapeutics(以下簡稱Nurix)簽下多年合作開發協議,希望藉由整合Seagen之ADC多年開發經驗、與Nurix的DELigase開發平臺,以及整合兩類藥物的優點,提供專一性更高、更有效、對正常組織毒性更小的新型藥物DACs (圖1)。根據協議,未來如果達到某些研究、開發、監管和商業里程碑,Seagen可能會額外支付高達34億美元的費用。Nurix保留對合作關係中產生的兩種產品進行聯合行銷和利潤分享的選擇權。
原名Seattle Genetics從1991年成立迄今,已與包含Amgen、Abbvie、Bayer、Genentech、Pfizer、Takeda等多家大藥廠合作開發ADCs,已有包含Adcetris、PADCEV、TIVDEAC三項產品上市。而Seagen的第一個ADC藥物,是與Takeda共同開發用於治療各種類型的淋巴瘤的Adcetris,目前正擴大在淋巴瘤以外的臨床試驗適應症,該藥已核准於全球65國銷售,有望在2023年成為暢銷藥物(年營收超過10億美元)。
Nurix則是成立於2012年的新興技術公司,專注包含靶向蛋白降解(Target Protein Degradation)或提升(Target Protein Elevation)的細胞內蛋白質調節(Target Protein Modulation)的藥物開發。目前已進入臨床開發藥物有兩項針對已產生抗藥性B細胞血癌的分子膠降解劑(Molecular glue degrader) NX-2127與NX-5948,以及拮抗CBL-B對B細胞活化抑制功能的小分子藥NX-1607,三項藥品都正於I期試驗階段。除與Seagen合作外,目前該公司也與Gilead、Sanofi共同開發藥物。
二、TPD發展正邁入成長期
2022年製藥產業在TPD掀起一股合作風潮,不僅國際知名大廠(如Amgen、GSK、Merck KGaA等)加碼參與,而且每宗合作案(含頭期款、研發里程碑金、商業化里程碑金、授權費用等)的總金額均上看5億美元以上,這顯示出這項技術正邁入成長期,並即將迎接廣泛應用和蓬勃發展的商業化時代。
TPD的發展較快主要有兩大類技術,其一PROTAC (Proteolysis targeting chimera),另一項則為分子膠(Molecular glue) (圖1)。截至2023年10月底,PROTAC約有190項以上產品開發中,在臨床試驗中(I~III期)就超過20項;分子膠類的蛋白降解劑有超過90項藥物發展中,在臨床試驗中(I~III期)就超過15項。
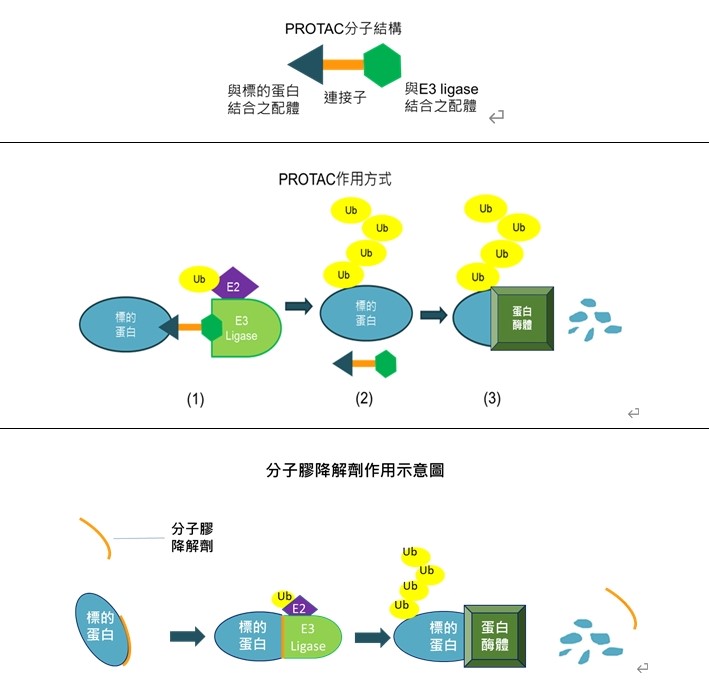
資料來源:工研院產科國際所 (2023/12)
圖1 TPD兩種主要標靶蛋白降解劑作用示意圖
三、Nurix的TPD理性藥物設計(Rational drug design)平臺,是獲得Seagen青睞的關鍵
2012年成立於加州舊金山的Nurix,聚焦設計可調節E3泛素連接酶(E3 ubiquitin ligase)功能的小分子藥物,透過對特定細胞內蛋白質 (E3 連接酶集合和 DNA 編碼的小分子庫)的提升或降解機制治療腫瘤。自成立到2020年共歷經A~D輪募資,總共募得1.68億美元。該公司在2020年6月公開上市,目前市值達2.9億美元。
Seagen主要是看上Nurix開發TPD經驗,與用於開發TPM之關鍵的理性藥物設計(Rational drug design) DELigase平臺技術(圖2),這個平臺有兩個重要關鍵組成-E3連接酶集合和DNA編碼的小分子庫(DNA Encoded Library, DEL)。人類基因體中有600多種E3連接酶,每種酶都有特定的功能。目前,標靶蛋白降解劑領域的開發主要集中在cereblon和VHL這兩種E3連接酶上。E3連接酶歷來被認為是不可成藥的,而Nurix在藥物發現過程中已利用60個E3連接酶。Nurix對E3連接酶的結構和功能的了解使能夠創建DNA編碼庫,專門用於識別利用或抑制E3連接酶的藥物。
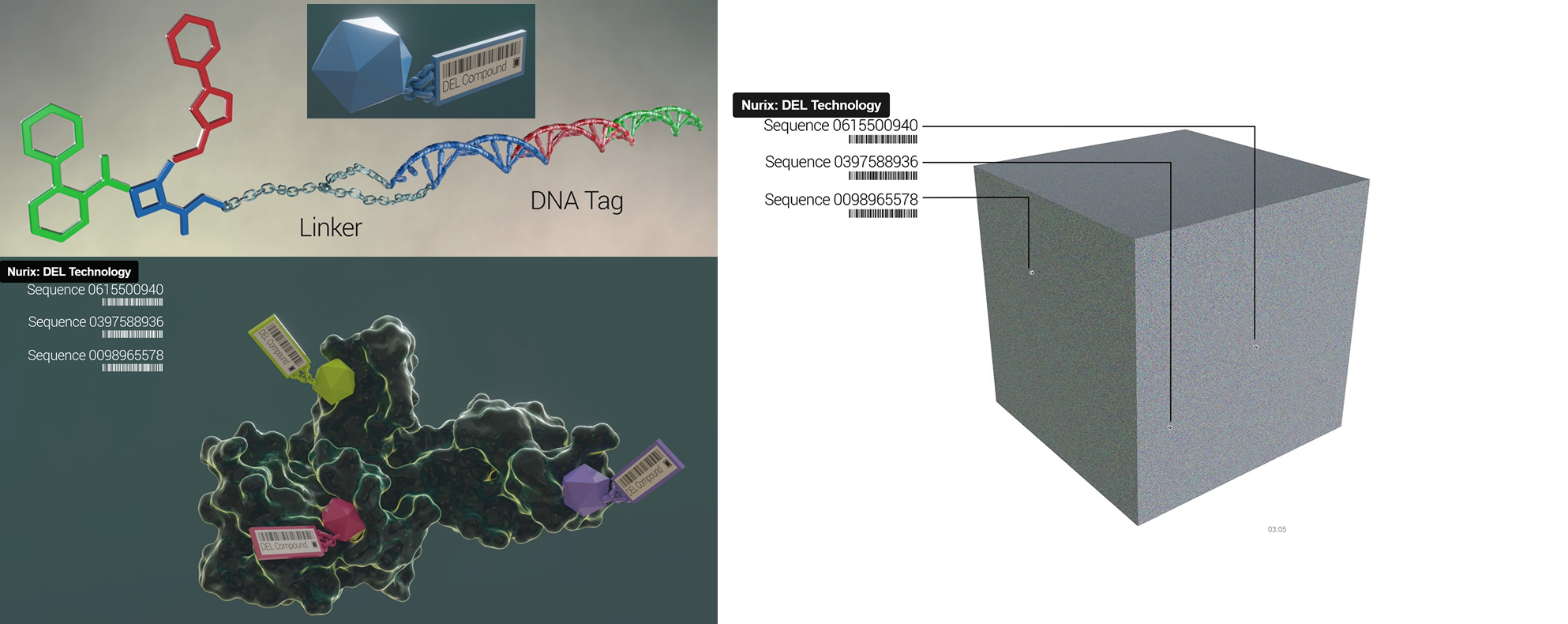
資料來源:公司官網(2023/10)
圖2 DELigase平臺,A:DNA編碼的小分子組成;B:DNA編碼的小分子與標的蛋白結合模擬;C:DEL電腦分析模型示意
Nurix的DNA編碼小分子庫是由超過50億個連接特定DNA編碼的小分子(圖2 A)組成,每個小分子都標有獨特的DNA條碼標籤。DEL作為混合物進行篩選,以識別與特定蛋白質標靶結合的小分子,而DNA標籤使得可用DNA定序技術快速識別微量的小分子(圖2 B)。Nurix透過其DNA編碼庫尋找目標蛋白和E3連接酶的結合物,為其標靶蛋白調節開發鑑別關鍵起始材料(圖2 C)。Nurix的DELigase方法在針對困難標靶進行快速藥物開發方面有多個優勢,特別是用於標靶蛋白調節劑等的連接酶開發。
透過結合Seagen對於抗體藥物複合物的多年實戰與成功上市經驗,Nurix在此次與Seagen的合作擬推進下一代ADCs的新治療類型DAC(圖3),將標靶蛋白降解劑 (TPD) 的催化活性與抗體的特異性相結合。這種新的治療方式有可能從兩個方面提高療效和提高安全性。首先,以降解劑取代劇毒的負載可以提高ADC的安全性和有效性。其次,DAC比傳統降解劑更具選擇性,因為DAC透過抗體導航可將降解劑專一地傳輸至特定腫瘤標的細胞。因此,透過將標靶蛋白降解劑技術與ADC結合,DAC有可能成為整合了標靶蛋白降解劑和當前ADC兩者優點的下一代替代品。
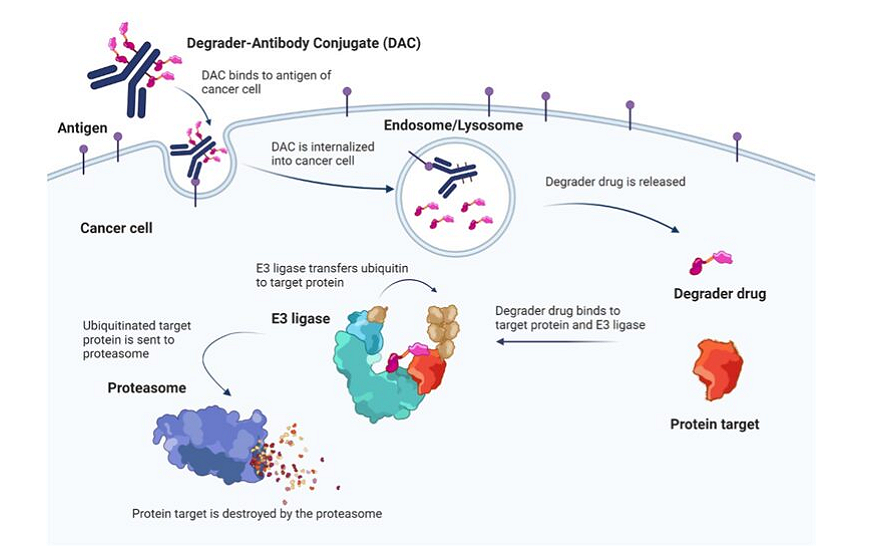
資料來源:公司官網(2023/10)
圖3 Degrader Antibody Conjugates (DAC)平臺與作用機制
四、目前國際開發相關產品中已有一項產品進入臨床I期
對於產業界來說,DAC是一項正在萌芽的技術。目前跑得最快的是韓國的Orum Therapeutics,已有1項產品正進行I期臨床試驗中,其餘均在臨床前的開發。以下簡要解析這些公司發展與其DAC候選產品發展狀況:
1.Orum Therapeutics
Orum Therapeutics 是一家成立於 2016 年、總部位於韓國大田的生物技術公司。聚焦開發針對細胞內蛋白的抗體工程藥物,以滿足癌症和罕見疾病中未滿足的醫療需求。公司專有技術利用一種名為 Oromab 的細胞穿透抗體平臺來抑制藥物標靶,並與知名CRO公司Schrödinger合作應用藥物化學、物理模擬等藥物資訊技術發展TPD2與TPS2(圖4)。Orum Therapeutics自2017年歷經6 輪募資,共籌集1億1,260萬美元的資金。他們最近一次融資是 2023 年 6 月進行的 2,010 萬美元的過渡融資(Bridge funding)。關鍵技術平臺包含TPD2 (Dual-precision Targeted Protein Degradation),應用發展結合在抗體上的DAC分子,目前有包含ORM-5029、ORM-1023、GSPT1-0001、ORM-6151(BMS-986497) 與PROTAb-0001;其中ORM-5029已於美國針對HER2陽性晚期乳癌進行I期臨床試驗,ORM-6151(BMS-986497)則於達成開發里程碑後在2023年11月7日被BMS以1.8億美元收購。另一項關鍵技術平臺則為TPS2 (Target Protein Stabilizer),有1項產品IO-0001,目前在早期研發階段。
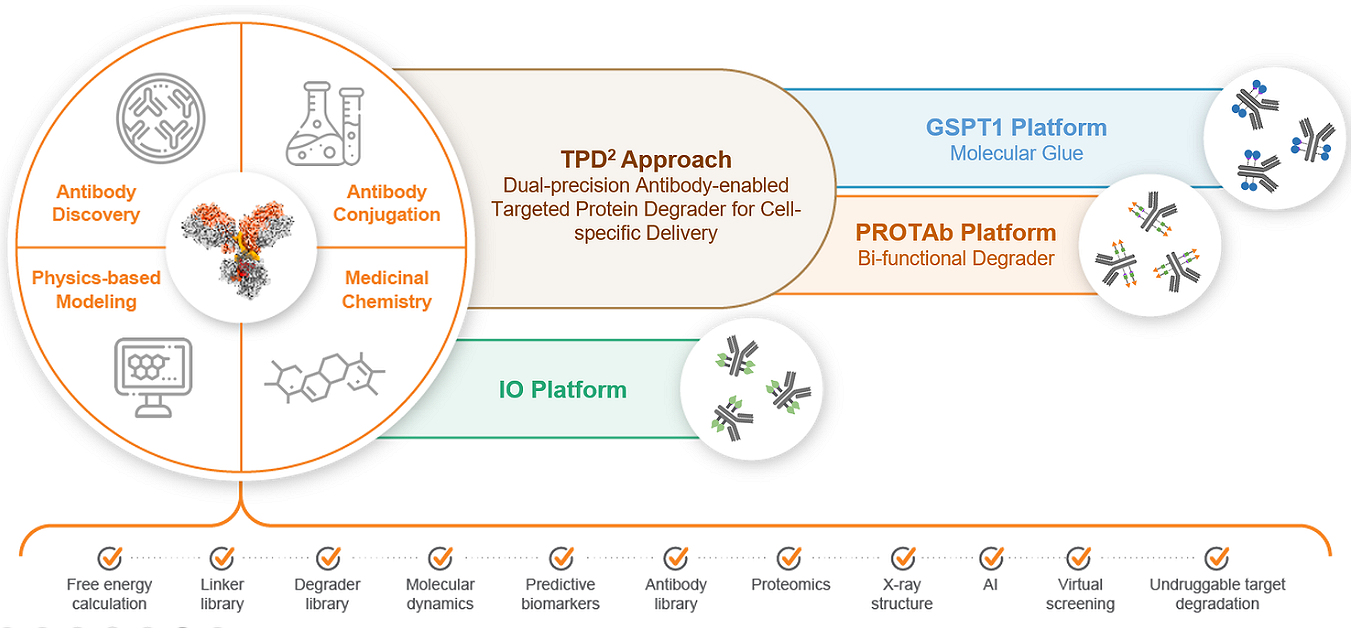
資料來源:公司官網(2023/10)
圖4 Orum的藥物開發引擎
2.Immunework, Inc.免疫功坊
由國際知名免疫學家張子文博士所創立的免疫功坊,2014年成立於臺灣臺北,2019年11月組織重組成立控股公司T-E Pharma Holding作為母公司,免疫功坊成為其全資子公司。免疫功坊的關鍵技術為同時具有標的部位(targeting moiety)與效應部位(effector moiety) 的T-E藥物平臺。其中標的部位可將藥物分子導向特定的組織、蛋白質或細胞,而效應部位負責執行預期的治療功能。這種設計概念可提升藥物的整體療效與安全性。而T-E藥物之標的部位與效應部位間透過多功能「多臂鏈接體」(multi-arm linkers),可使T-E藥物接上2個以上的小分子,成為「滿載多臂鏈接體」(packed multi-arm linkers),以創建出各樣新藥分子,包含抗體藥物複合物(antibody-drug conjugates, ADCs)、抗體放射性核種複合物(antibody-radionuclide conjugates, ARCs)、超長效胜肽藥物與DAC等,應用於廣泛的臨床範疇。該公司於2022年3月完成A輪資金2,400萬美元的募資,目前DAC候選藥物TE-1146已授權同屬T-E Pharma Holding的締醫生技(T-E Meds, Inc.)進行後續商業開發。根據免疫功坊的試驗資料顯示,TE-1146具有良好的體內與體外穩定性,在細胞試驗、小鼠動物模式中僅需相較於一線用藥Lenalidomide (屬於分子膠類)更少劑量(約千分之一)即可達到相當的抗多發性骨髓瘤(multiple myeloma)效果。
3.Bioloomics Inc.
Bioloomics是在DARPA資助科羅拉多大學Boulder分校的Rapid Threat Assessment (RTA)計畫中進行了七年的有關生物感測技術研究後於2019年成立的新創公司。該公司在參與RTA計畫時發現利用複雜的成像和自動化細胞挑選的”單細胞測試”在抗體定向演化(directed evolution)方面具有巨大的潛力,該公司將之發展為整合合成生物學、機器人、AI影像分析等技術的高通量篩選FERT Biosensor平臺,可在短短一天內篩查10萬種以上的藥物。通常R&D到候選藥物的開發時間約需要6年左右,而根據Bioloomics的資料,使用FERT Biosensor平臺技術可以將時程縮短到1~1.5年。
Bioloomics迄今種子輪募資,共募得935萬美元,將以FERT Biosensor技術發展聚焦可標靶細胞內胞器(如溶酶體(lysosome)、內質網(Endoplasmic Reticulum)、高基氏體(Golgi apparatus))的抗體發展腫瘤藥物,目前尚處早期研發階段。
五、結論
精準藥物的發展在大、小分子技術進步下,不斷推出新作,本文所提及DAC更是搶在標靶蛋白降解劑 (TPD)發展成熟前所發展的次世代產品。新世代抗體工程藥物發展也因為新藥物技術的加入而變得更多元,從最早的ADCs、AOC 、演變到本文所提及的DAC,無不是以抗體為導向載體,攜帶多元、具特異性的創新載荷(payload),以發展在多重專一性加持下,副作用更小的精準療法。而從Nurix、Orum、與Bioloomics的發展平台技術中,除了擁有龐大藥物組成元件庫外,我們看到這些公司不約而同透過ICT、自動化等智慧技術使用,使能快速從龐大的藥物元件庫中篩出最佳組合,縮減開發時程及早搶進臨床開發。顯見藥物開發單靠傳統方式已遠遠不足,善用資訊與自動化科技輔助,將有效加速創新藥物開發,協助搶得先機。
(本文作者為工研院產科國際所執行產業技術基磐研究與知識服務計畫產業分析師)
 點閱數
點閱數:
189

